Aufgabenstellung:
In einem Behälter mit reibungsfrei verschiebbarem Kolben befinde sich bei einem Druck von
a) Welche Stoffmenge
b) Welche mittlere Geschwindigkeit (Wurzel aus dem mittleren Geschwindigkeitsquadrat) hat ein Stickstoff-Molekül?
c) Welches Volumen
Das Gas wird nun auf die Temperatur
d) Skizzieren Sie diese Zustandsänderung in einem
e) Welche Arbeit
Molmasse
Ein Stickstoffmolekül soll als starre Hantel behandelt werden,
Lösungsweg:
(a) Stoffmenge
Die Stoffmenge
Für ein ideales Gas ist die Innere Energie
Die Innere Energie
Jedem Freiheitsgrad wird nach dem Gleichverteilungssatz der Energie die gleiche thermische Energie zugeordnet.
Nimmt man für die zweiatomigen Moleküle des Stickstoffs an, dass im betrachteten Temperaturbereich auch die Freiheitsgrade der Rotation angeregt sind, dann ist die Anzahl der Freiheitsgrade
Man erhält damit für den Anfangszustand ' 1 '
(b) mittlere Geschwindigkeit
Für das Modell des idealen Gases liefert die kinetische Theorie als mittlere kinetische Energie
dabei ist
Die Masse
oder alternativ aus der relativen Molekülmasse
Damit ist das mittlere Geschwindigkeitsquadrat für den Zustand ' 1 '
Definitionsgemäß wird damit die mittlere Geschwindigkeit (Wurzel aus dem mittleren Geschwindigkeitsquadrat)
(c) Volumen
Aus der Zustandsgleichung eines idealen Gases folgt
Die Dichte
erhält man für die Dichte
Lösungsvariante
Die kinetische Gastheorie liefert den Zusammenhang zwischen den makroskopischen Größen der Dichte
Mit den Zustandsgrößen für den Zustand ' 1 ' wird
(d)
Im
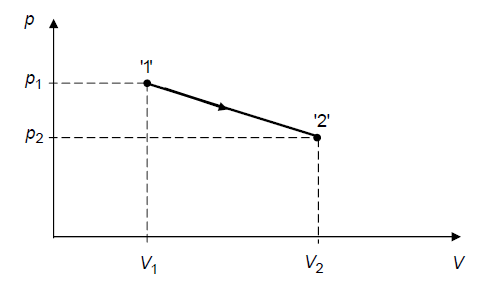
(e)
Die Zustände ' 1 und '2' sind jeweils gekennzeichnet durch Druck, Temperatur und Volumen.
Anfangszustand ' 1 '
Die Zustandsgleichung eines idealen Gases gilt für den Anfangszustand ' 1 ' und der Endzustand ' 2 ', also
und
oder nach Division der beiden Gleichungen durcheinander
Bei der Expansion ' 1 '
Die abgegebene Arbeit wird (das Vorzeichen mit einbezogen)
Die Änderung
Die molare isochore Wärmekapazität
damit wird
Das Minus-Vorzeichen besagt, dass sich bei diesem Prozess die Innere Energie absenkt.
Der 1. Hauptsatz der Wärmlehre verknüpft die Änderung der Inneren Energie
daraus erhält man die beim Prozess ' 1 '
Das Minus-Vorzeichen besagt, dass bei diesem Prozess Wärme vom System abgegeben wird.
Lösung:
-
-
-
-
siehe Musterlösung
-