Aufgabenstellung:
Ein HCl-Molekül kann sowohl zu Schwingungen als auch zu Rotationen angeregt werden. Die Energie der Schwingungs-Rotations-Zustände ist gegeben durch
-
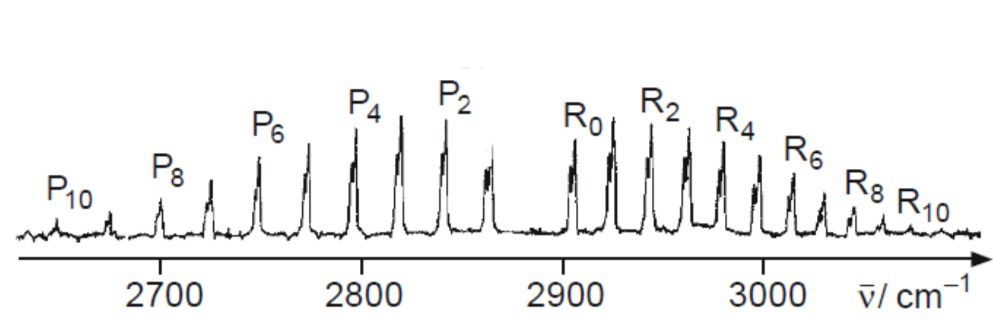
In der Abbildung sehen Sie ein gemessenes Spektrum von Schwingungsrotationszuständen. Es zerfällt in zwei Teile, den P-Zweig und den R-Zweig. Was charakterisiert P- bzw. R-Übergänge? Zeichnen Sie alle erlaubten Übergänge in ein Energieniveauschema für
und . Warum gibt es keinen Peak bei ? Hinweis:
-
Entwickeln Sie eine Formel für die reziproke Wellenlänge
in Abhängigkeit des Drehimpulses und des Abstands der Atome.
Hinweis: Das Rotationsträgheitsmomenthängt klassisch von der reduzierten Masse und dem Abstand zweier Körper ab. -
Berechnen Sie wie groß der Abstand R zwischen den beiden Atomen im Molekül ist
Bestimmen Sie dazu den mittleren Abstand der Absorptionspeaks aus der Messung.
Lösungsweg:
a) Charakterisierung von P- bzw. R-Übergängen, Termschema:

Für den P-Zweig gilt
Der Übergang
b) Reziproke Wellenlänge
Die Energie eines Rotationszustandes hängt vom Erwartungswert des Gesamtdrehimpulses ab.
Man erhält dann für den Abstand zweier benachbarter Niveaus
Nach Kürzen von Konstanten und Umstellen ergibt sich
c) Abstand R zwischen den beiden Atomen im Molekül
Der Abstand zwischen zwei benachbarten Absorptionspeaks kann aus der Formel aus Aufgabe b hergeleitet werden.
Daraus lässt sich eine Formel für den Kernabstand ableiten
Mit
Lösung:
- Für den P-Zweig gilt
; für den R-Zweig .